











一、大腸埃希氏菌簡介
大腸埃希氏菌(Escherichia coli)又稱大腸杆菌,廣泛存在於人和溫血動物的腸道中,能夠在44.5℃發酵乳糖產酸產氣,IMViC(靛基質、甲基紅、VP試驗、檸檬酸鹽)生化試驗結果為++--或-+--的革蘭氏陰性杆菌。以此作為糞便汙染指標來評價食品的衛生狀況,推斷食品中腸道致病菌汙染的可能性。
二、參考標準
《GB 4789.38-2012 食品安全國家標準 食品微生物學檢驗 大腸埃希氏菌計數》。
三、檢驗流程
(一)MPN法
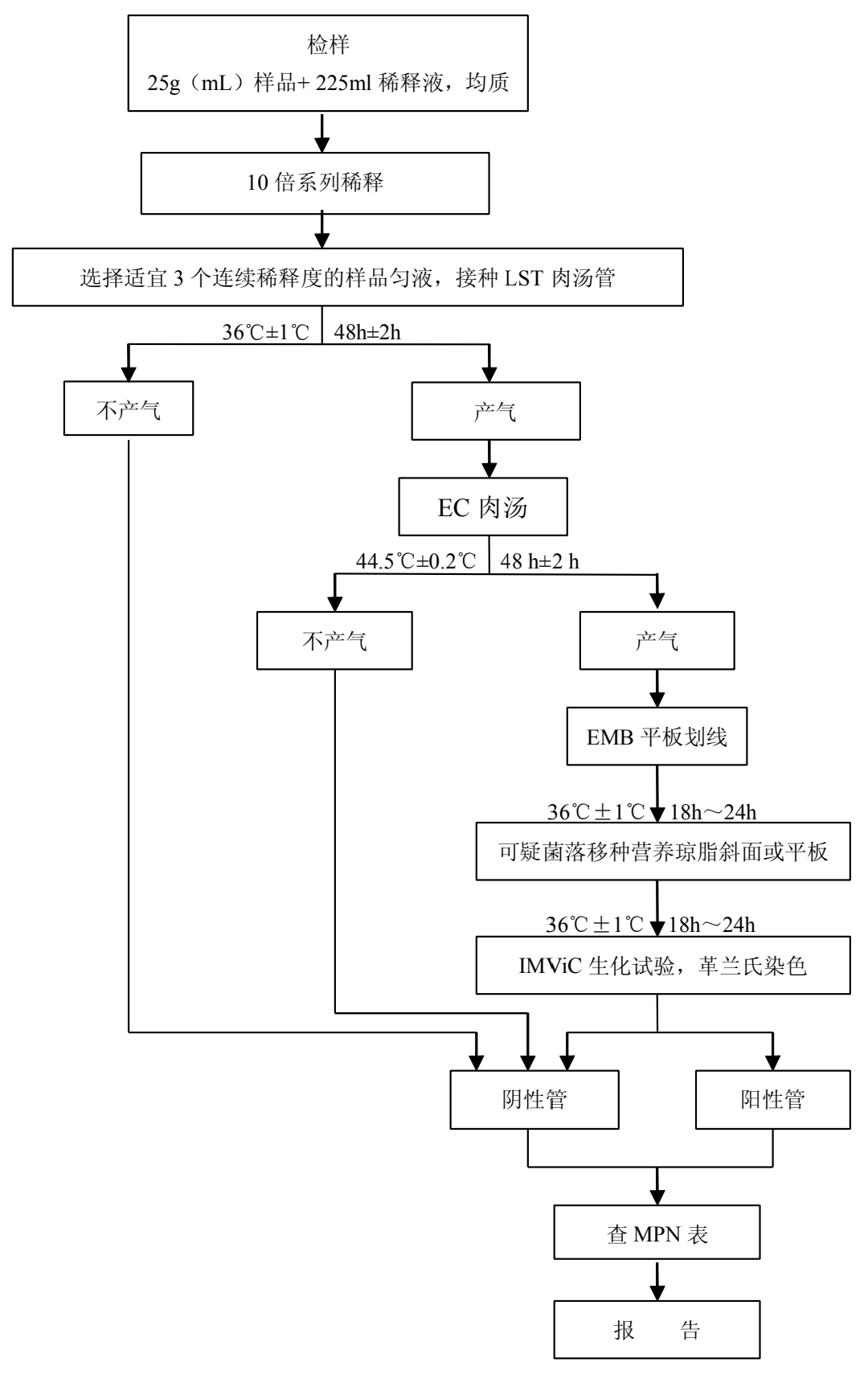
圖1 大腸埃希氏菌MPN計數法檢驗程序
1.初發酵試驗
每個樣品,選擇3個適宜的連續稀釋度的樣品勻液(液體樣品可以選擇原液),每個稀釋度接種3管月桂基硫酸鹽胰蛋白腖(LST)肉湯,每管接種1mL(如接種量超過1mL,則用雙料LST肉湯),36±1℃培養24±2h,觀察小倒管內是否有氣泡產生,24±2h產氣者進行複發酵試驗,如未產氣則繼續培養48±2h。產氣者進行複發酵試驗。如所有LST肉湯管均未產氣,即可報告大腸埃希氏菌MPN結果。
根據標準菌株對月桂基硫酸鹽胰蛋白腖(LST)肉湯進行驗證。大腸菌群、大腸杆菌和發酵乳糖的革蘭氏陰性細菌產生氣體,在小倒管內有氣泡;其它細菌無氣泡。結果如圖2所示:
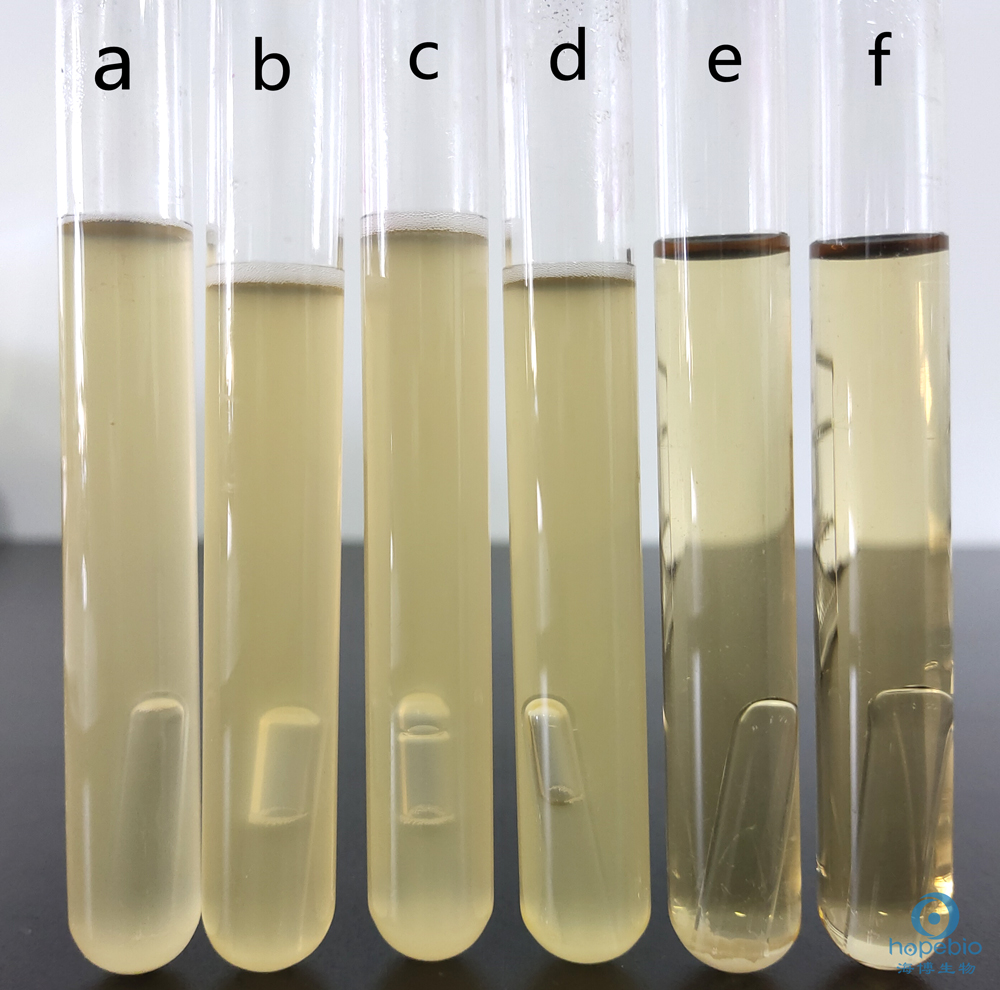
a:鼠傷寒沙門氏菌 b:大腸埃希氏菌 c:弗氏檸檬酸杆菌 d:陰溝腸杆菌 e:糞腸球菌 f:空白對照
圖2 月桂基硫酸鹽胰蛋白腖(LST)肉湯微生物質控結果
2.複發酵試驗
用接種環從產氣的LST肉湯管中分別取培養物1環,移種於已提前預溫至45℃的EC肉湯管中,放入帶蓋的44.5±0.2℃水浴箱內。水浴的水麵應高於肉湯培養基液麵,培養24±2h,檢查小倒管內是否有氣泡產生,如未有產氣則繼續培養至48±2h。記錄在24h和48h內產氣的EC肉湯管數。如所有EC肉湯管均未產氣,即可報告大腸埃希氏菌MPN結果;如有產氣者,則進行EMB平板分離培養。
根據標準菌株對EC肉湯進行驗證。糞大腸菌群和大腸杆菌產生氣體,在倒立小發酵管中有氣泡。結果如圖3所示:
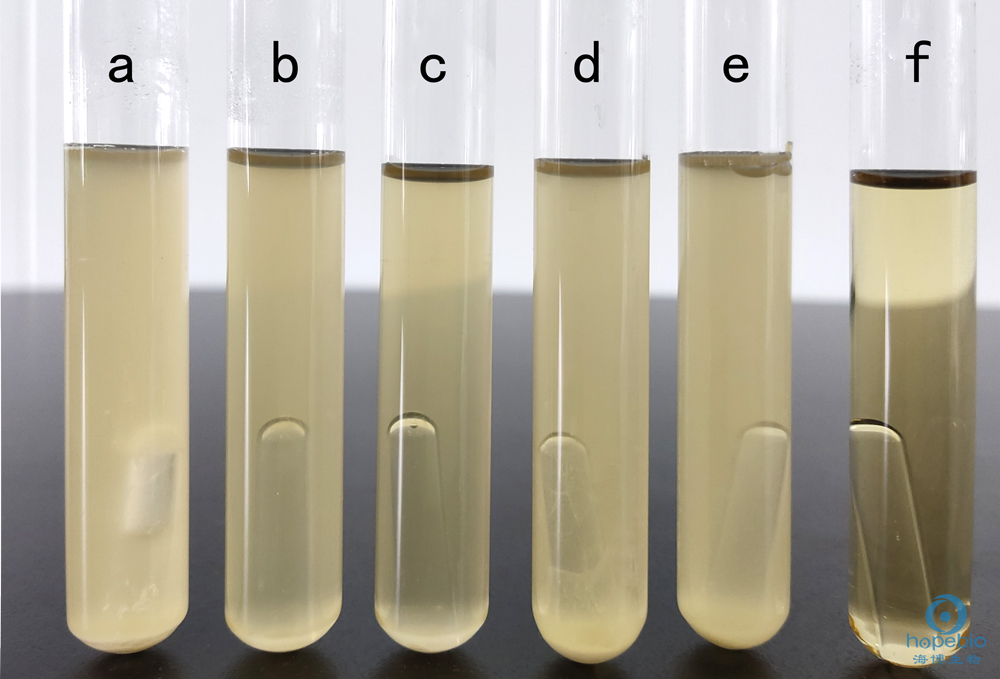
a:大腸埃希氏菌菌 b:鼠傷寒沙門氏菌 c:弗氏檸檬酸杆菌 d:陰溝腸杆菌 e:肺炎克雷伯氏菌 f:空白對照
圖3 EC肉湯微生物質控結果
3.伊紅美藍(EMB)平板分離培養
輕輕振搖各產氣管,用接種環取培養物分別劃線接種於EMB平板,36±1℃培養18~24h。觀察平板上有無具黑色中心有光澤或無光澤的典型菌落。
根據標準菌株對EMB培養基進行驗證。典型大腸埃希氏菌菌落特征為具黑色中心有金屬光澤,產氣腸杆菌為粉紅色菌落無光澤,鼠傷寒沙門氏菌為無色菌落。結果如圖4所示:

a:大腸埃希氏菌 b:產氣腸杆菌 c:鼠傷寒沙門氏菌
圖4 EMB培養基微生物質控結果
4.革蘭氏染色
挑取營養瓊脂培養基上的純培養的單個可疑菌落,進行革蘭氏染色。大腸埃希氏菌為革蘭氏陰性無芽胞杆菌,呈紅色杆狀。結果如圖5所示:
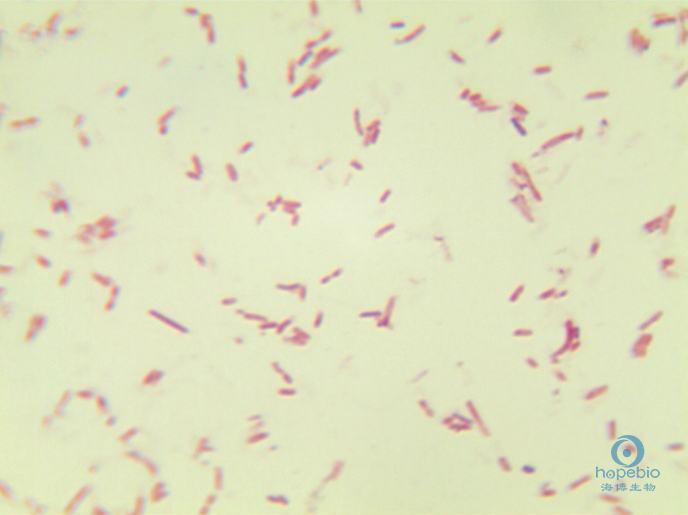
圖5 大腸埃希氏菌的革蘭氏染色結果
5.生化鑒定
取培養物進行靛基質試驗、甲基紅試驗、VP試驗和檸檬酸鹽利用試驗,可選取使用大腸杆菌生化鑒定條進行生化鑒定,大腸埃希氏菌的生化反應結果為靛基質陽性、甲基紅陽性、VP陰性、檸檬酸鹽陰性。如圖6所示:

圖6 大腸埃希氏菌生化鑒定條試驗結果
6.結果判定
大腸埃希氏菌為革蘭氏陰性無芽胞杆菌,發酵乳糖、產酸、產氣,IMViC生化試驗為++--或-+--。隻要有1個菌落鑒定為大腸埃希氏菌,其所代表的LST肉湯管即為大腸埃希氏菌陽性。依據LST肉湯陽性管數查MPN表,報告每g(mL)樣品中大腸埃希氏菌MPN值。
(二)平板計數法
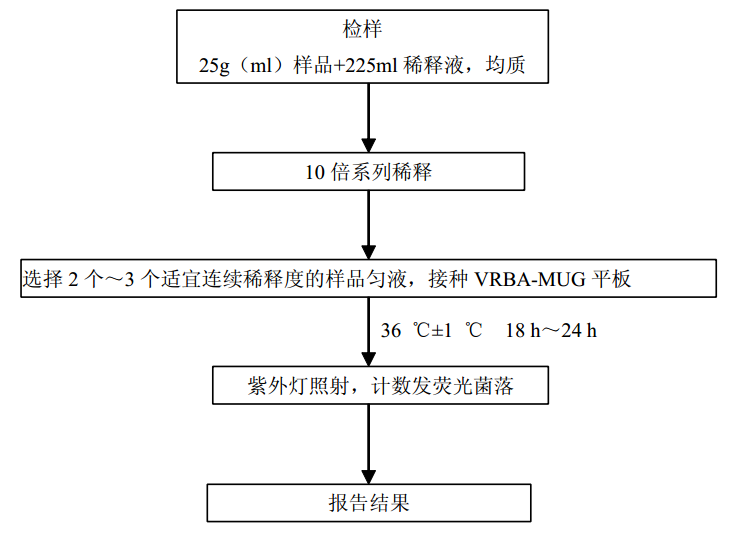
圖7 大腸埃希氏菌平板計數法檢驗程序
1.平板計數
取2~3個適宜的連續稀釋度的樣品勻液,每個稀釋度接種2個無菌平皿, 每皿1mL。同時取1mL稀釋液加入無菌平皿做空白對照。
將10~15 mL 冷至45±0.5℃的結晶紫中性紅膽鹽瓊脂(VRBA)傾注於每個平皿中。小心旋轉平皿,將培養基與樣品勻液充分混勻。待瓊脂凝固後,再加3~4 mL VRBA-MUG覆蓋平板表層。凝固後翻轉平板,36±1℃培養18~24 h。
根據標準菌株對VRBA培養基進行驗證,大腸埃希氏菌為紫紅色菌落,有膽鹽沉澱環;在紫外燈照射下有熒光。結果如圖8所示:
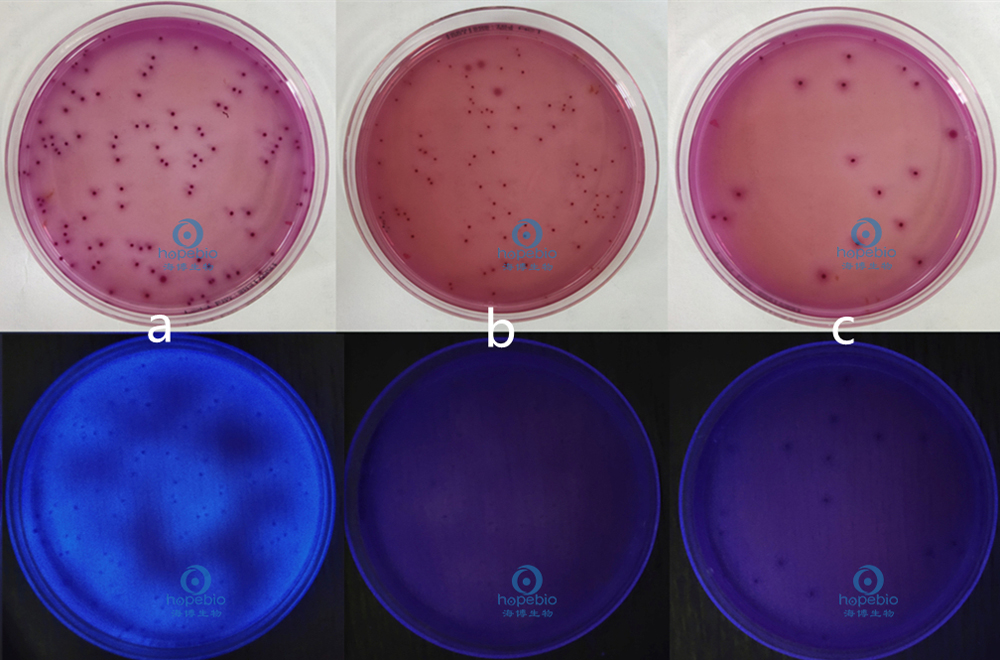
a;大腸埃希氏菌 b;弗氏檸檬酸杆菌 c;陰溝腸杆菌
圖8 VRBA培養基微生物質控結果
注意事項:選擇菌落數在10~100CFU之間的平板,暗室中360~366nm波長紫外燈照射下,計數平板上發淺藍色熒光的菌落。
2.結果判定
兩個平板上發熒光菌落數的平均數乘以稀釋倍數,報告每g(mL)樣品中大腸埃希氏菌數,以CFU/g(mL)表示。若所有稀釋度(包括液體樣品原液)平板均無菌落生長,則以小於1乘以最低稀釋倍數報告。
注:本文屬betway必威西汉姆联生物原創,未經允許不得轉載。
上一篇:食品中誌賀氏菌的檢驗(下)
下一篇:葉酸測定培養基試驗方法及注意事項

