











1 範圍
本標準規定了食品中產氣莢膜梭菌(Clostridium perfringens)的檢驗方法。
本標準適用於食品中產氣莢膜梭菌的檢驗。
2 設備和材料
除微生物實驗室常規滅菌及培養設備外,其他設備和材料如下:
a) 恒溫培養箱:36 ℃±1 ℃;
b) 冰箱:2 ℃~5℃;
c) 恒溫水浴箱:50℃±1 ℃,46℃±0.5℃;
d) 天平:感量0.1 g;
e) 均質器;
f) 顯微鏡:10×~100×;
g) 無菌吸管:1 mL(具0.01 mL 刻度)、10 mL(具0.1 mL 刻度)或微量移液器及吸頭;
h) 無菌試管:18mm×180mm;
i) 無菌培養皿:直徑90 mm;
j) pH 計或pH 比色管或精密pH 試紙;
k) 厭氧培養裝置。
3 培養基和試劑
3.1 胰腖-亞硫酸鹽-環絲氨酸(TSC)瓊脂:見附錄A 中A.1。
3.2 液體硫乙醇酸鹽培養基(FTG):見附錄A 中A.2。
3.3 緩衝動力-硝酸鹽培養基:見附錄A 中A.3。
3.4 乳糖-明膠培養基:見附錄A 中A.4。
3.5 含鐵牛乳培養基:見附錄A 中A.5。
3.6 0.1%蛋白腖水:見附錄A 中A.6。
3.7 革蘭氏染色液:見附錄A 中A.7。
3.8 硝酸鹽還原試劑:見附錄A 中A.8。
3.9 緩衝甘油-氯化鈉溶液:見附錄A 中A.9。
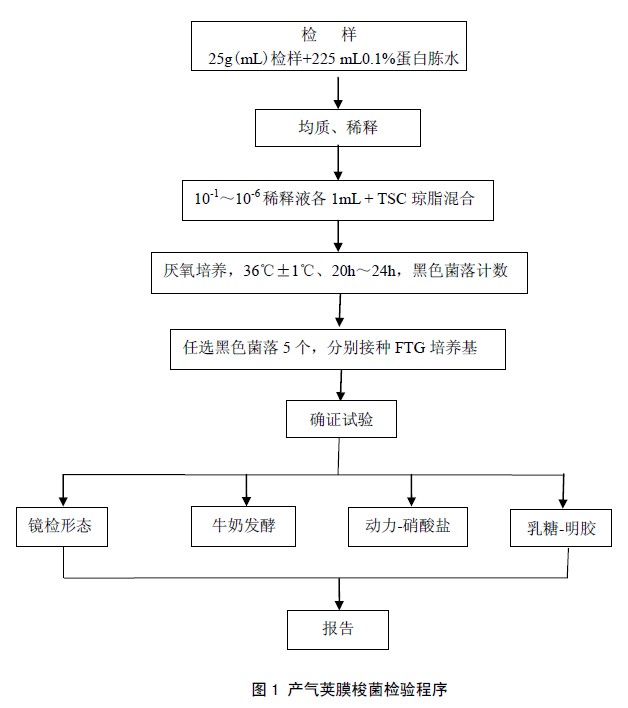
4 檢驗程序
產氣莢膜梭菌檢驗程序見圖1。
5 操作步驟
5.1 樣品製備
5.1.1 樣品采集後應盡快檢驗,若不能及時檢驗,可在2 ℃~5 ℃保存;如8 h 內不能進行檢驗,應以
無菌操作稱取25 g(mL)樣品加入等量緩衝甘油-氯化鈉溶液(液體樣品應加雙料),並盡快至於-60 ℃
低溫冰箱中冷凍保存或加幹冰保存。
5.1.2 以無菌操作稱取25 g(mL)樣品放入含有225 mL 0.1%蛋白腖水(如為5.1.1 中冷凍保存樣品,
室溫解凍後,加入200 mL 0.1%蛋白腖水)的均質袋中,在拍擊式均質器上連續均質1 min~2 min;或
置於盛有225 mL0.1%蛋白腖水的均質杯中,8 000 r/min~10 000 r/min 均質1min~2 min,作為1:10 稀釋
液。
5.1.3 以上述1:10 稀釋液按1 mL 加0.1%蛋白腖水9 mL 製備10-2~10-6 的係列稀釋液。
5.2 培養
5.2.1 吸取各稀釋液1 mL 加入無菌平皿內,每個稀釋度做兩個平行。每個平皿傾注冷卻至50 ℃的TSC
瓊脂(可放置於50 ℃±1 ℃恒溫水浴箱中保溫)15 mL,緩慢旋轉平皿,使稀釋液和瓊脂充分混勻。
5.2.2 上述瓊脂平板凝固後,再加10 mL 冷卻至50 ℃的TSC 瓊脂(可放置於50 ℃±1 ℃恒溫水浴箱
中保溫)均勻覆蓋平板表層。
5.2.3 待瓊脂凝固後,正置於厭氧培養裝置內,36 ℃±1 ℃培養20 h~24 h。
5.2.4 典型的產氣莢膜梭菌在TSC 瓊脂平板上為黑色菌落。
5.3 確證試驗
5.3.1 從單個平板上任選5 個(小於5 個全選)黑色菌落,分別接種到FTG 培養基,36 ℃±1 ℃培養
18 h~24 h。
5.3.2 用上述培養液塗片,革蘭氏染色鏡檢並觀察其純度。產氣莢膜梭菌為革蘭氏陽性粗短的杆菌,有
時可見芽孢體。如果培養液不純,應劃線接種TSC 瓊脂平板進行分純,36 ℃±1 ℃厭氧培養20 h~24 h,
挑取單個典型黑色菌落接種到FTG 培養基,36 ℃±1 ℃培養18 h~24 h,用於後續的確證試驗。
5.3.3 取生長旺盛的FTG 培養液1 mL 接種於含鐵牛乳培養基,在46 ℃±0.5 ℃水浴中培養2 h 後,每
小時觀察一次有無“暴烈發酵”現象,該現象的特點是乳凝結物破碎後快速形成海綿樣物質,通常會上
升到培養基表麵。5 h 內不發酵者為陰性。產氣莢膜梭菌發酵乳糖,凝固酪蛋白並大量產氣,呈“暴烈發
酵”現象,但培養基不變黑。
5.3.4 用接種環(針)取FTG 培養液穿刺接種緩衝動力-硝酸鹽培養基,於36 ℃±1 ℃培養24 h。在透
射光下檢查細菌沿穿刺線的生長情況,判定有無動力。有動力的菌株沿穿刺線呈擴散生長,無動力的菌
株隻沿穿刺線生長。然後滴加0.5 mL 試劑甲和0.2 mL 試劑乙以檢查亞硝酸鹽的存在。15 min 內出現紅
色者,表明硝酸鹽被還原為亞硝酸鹽;如果不出現顏色變化,則加少許鋅粉,放置10 min,出現紅色者,
表明該菌株不能還原硝酸鹽。產氣莢膜梭菌無動力,能將硝酸鹽還原為亞硝酸鹽。
5.3.5 用接種環(針)取FTG 培養液穿刺接種乳糖-明膠培養基,於36 ℃±1 ℃培養24 h,觀察結果。
如發現產氣和培養基由紅變黃,表明乳糖被發酵並產酸。將試管於5 ℃左右放置1 h,檢查明膠液化情況。
如果培養基是固態,於36 ℃±1 ℃再培養24 h,重複檢查明膠是否液化。產氣莢膜梭菌能發酵乳糖,使
明膠液化。
6 結果與報告
6.1 典型菌落計數
選取典型菌落數在20 CFU~200 CFU 之間的平板,計數典型菌落數。如果:
a) 隻有一個稀釋度平板的典型菌落數在20CFU~200CFU 之間,計數該稀釋度平板上的典型菌落;
b)最低稀釋度平板的典型菌落數均小於20 CFU,計數該稀釋度平板上的典型菌落;
c)某一稀釋度平板的典型菌落數均大於200 CFU,但下一稀釋度平板上沒有典型菌落,應計數該稀
釋度平板上的典型菌落;
d)某一稀釋度平板的典型菌落數均大於200 CFU,且下一稀釋度平板上有典型菌落,但其平板上的
典型菌落數不在20 CFU~200 CFU 之間,應計數該稀釋度平板上的典型菌落;
e)2 個連續稀釋度平板的典型菌落數均在20CFU~200CFU 之間,分別計數2 個稀釋度平板上的典
型菌落。
6.2 結果計算
6.1 計數結果按公式(1)計算:
式中:
T——樣品中產氣莢膜梭菌的菌落數;
A——單個平板上典型菌落數;
B——單個平板上經確證試驗為產氣莢膜梭菌的菌落數;
C——單個平板上用於確證試驗的菌落數;
n1 ——第一稀釋度(低稀釋倍數)經確證試驗有產氣莢膜梭菌的平板個數;
n2 ——第二稀釋度(高稀釋倍數)經確證試驗有產氣莢膜梭菌的平板個數;
0.1——稀釋係數;
d——稀釋因子(第一稀釋度)。
6.3 報告
根據TSC 瓊脂平板上產氣莢膜梭菌的典型菌落數,按照6.2 中公式計算,報告每g(mL)樣品中產
氣莢膜梭菌數,報告單位以CFU/ g(mL)表示;如T 值為0,則以小於1 乘以最低稀釋倍數報告。
上一篇:CMA/CNAS/CAL區別

