











一、陰溝腸杆菌簡介
陰溝腸杆菌(Enterobacter cloacae)是腸杆菌科腸杆菌屬的模式菌,廣泛分布於自然界,普遍存在於人和動物的腸道中,是醫院內感染和機會感染的常見細菌,也能引起食源性疾病,因此常常被當作條件致病菌的代表。
奶粉中陰溝腸杆菌的汙染一直受到人們的關注,2004年4月,聯合國糧農組織和世界衛生組織的專家在評估嬰兒配方奶粉安全性時,認為陰溝腸杆菌在引起新生兒致病方麵的重要性正在增長,並且作為腸杆菌屬的代表(在嬰兒奶粉中以低濃度出現的)是潛在的嬰兒奶粉病原菌,在進行嬰兒配方奶粉中致病菌的風險分析時,將陰溝腸杆菌列為“B”類危險性生物因子。
據調查報告表明奶粉中汙染陰溝腸杆菌的含量一般較低,為此本方法定量檢測取樣量確定為333 g,以盡可能檢測出樣品中含量少的目標菌。
二、參考標準
《SN/T 2552.7-2010 乳與乳製品衛生微生物學檢驗方法 第7部分:陰溝腸杆菌檢驗》
三、陰溝腸杆菌檢驗方法
3.1 方法提要
奶粉中陰溝腸杆菌的分離與計數方法是應用微生物檢驗的增菌培養、分離、生化鑒定等方法對奶粉中可能存在的陰溝腸杆菌進行定性和定量的檢驗。
3.2 檢驗程序
陰溝腸杆菌的檢驗程序見圖1。
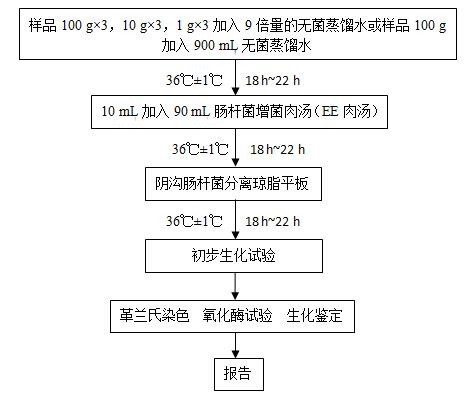
圖1 陰溝腸杆菌檢驗程序
四、檢測步驟及結果判斷
4.1陰溝腸杆菌定量檢驗(MPN法)
4.1.1 定量檢驗是應用“三管”增菌法,檢驗和定量樣品中極少量的陰溝腸杆菌。檢驗需333g樣品。取樣見SN/T 2552.1。
4.1.2 取樣前消毒樣品包裝的開啟處和取樣勺,無菌稱取樣品100g、10g和1g各三份分別加入2L、250mL和125mL樣品稀釋瓶中,在各樣品稀釋瓶中分別加入900mL、90mL、9mL預熱到45℃的滅菌蒸餾水(1:10稀釋),振搖使樣品充分混勻,36℃±1℃培養18h~22h。
4.1.3 分別移取培養18h~22h的懸液各10mL加入90mLEE肉湯中,36℃±1℃培養18h~22h。
腸道菌增菌肉湯(EE)檢驗原理:蛋白腖為微生物生長提供蛋白質、維生素和氨基酸;葡萄糖提供碳源;磷酸氫二鈉和磷酸二氫鉀為緩衝劑;牛膽鹽和煌綠為選擇性抑菌劑,可抑製非腸杆菌科細菌的生長。
腸道菌增菌肉湯(EE)用法:稱取本品45g,加熱攪拌溶解於1000mL蒸餾水中,分裝三角瓶,每瓶90mL,100℃加熱30分鍾,迅速在流動的冷水中冷卻,無需高壓滅菌。培養結果如圖2所示:

圖2 陰溝腸杆菌在EE肉湯中的培養結果
4.1.4 輕輕混勻增菌液,用下列方法進行平板接種:
直接塗布法:每份增菌液取0.2mL加到2個陰溝腸杆菌分離瓊脂平板(ECIA),每個平板0.1mL,用無菌玻璃塗布棒塗布(如果預計奶粉中含有大量的細菌,應使用滅菌的EE肉湯將增菌液稀釋10-4~10-6後塗布)。
直接劃線法:每份增菌液用3mm接種環(10μL)分別接種2個陰溝腸杆菌分離瓊脂平板,三區法或四區法劃線,以得到單個菌落。將平板倒置於36℃±1℃,培養18h~22h。
陰溝腸杆菌分離瓊脂(ECIA)檢驗原理:特殊蛋白腖為微生物的生長提供氮源、維生素和生長因子;氯化鈉維持均衡的滲透壓;3號膽鹽和結晶紫為抑菌劑;溴麝香草酚藍為pH指示劑,變色範圍為pH值6.0~7.6,酸性呈黃色,堿性呈藍色;棉子糖為可發酵糖類,發酵糖產酸的菌落呈黃色;瓊脂是培養基的凝固劑。
陰溝腸杆菌分離瓊脂(ECIA)用法:稱取本品49.6g,加熱煮沸溶解於1000mL蒸餾水中,冷卻至50℃左右時,傾入無菌平皿,備用。無需高壓滅菌。培養結果如圖3所示:
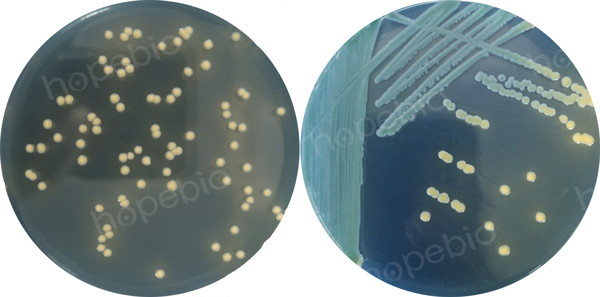
圖3 陰溝腸杆菌在ECIA平板上的培養結果
4.1.5 觀察平板上陰溝腸杆菌的典型形態
在陰溝腸杆菌分離瓊脂平板上:黃色菌落,圓形,凸起,直徑2mm~3mm。
4.1.6 從陰溝腸杆菌分離瓊脂平板上挑取5個可疑菌落,分別進行初步生化試驗:賴氨酸脫羧酶、鳥氨酸脫羧酶、精氨酸雙水解酶試驗。初步生化試驗結果如圖4:

圖4 初步生化實驗結果
4.1.7 對賴氨酸脫羧酶陰性、鳥氨酸脫羧酶陽性、精氨酸雙水解酶陽性的可疑菌落,進行革蘭氏染色,氧化酶試驗。革蘭氏染色陰性,氧化酶試驗陰性按表1進行生化試驗。革蘭氏染色結果如圖5,氧化酶試驗結果如圖5:

圖5 陰溝腸杆菌革蘭氏染色結果,陰溝腸杆菌氧化酶實驗結果
4.1.8 腸杆菌屬細菌生化特征見表1。生化試驗結果如圖6所示。
表1 腸杆菌屬細菌生化特征
|
試驗 |
生化特征 |
|||||
|
陰溝腸杆菌 E.cloacae |
阪崎腸杆菌 E.sakazakii |
產氣腸杆菌 E.aerogenes |
聚團腸杆菌 E.agglomerans |
格高菲腸杆菌 E.gergoviae |
||
|
賴氨酸脫酸酶 |
- |
- |
+ |
- |
+ |
|
|
精氨酸雙水解酶 |
+ |
+ |
- |
- |
- |
|
|
鳥氨酸脫酸酶 |
+ |
+ |
+ |
- |
+ |
|
|
發酵 |
KCN生長 |
+ |
+ |
+ |
v |
- |
|
蔗糖 |
+ |
+ |
+ |
(+) |
+ |
|
|
衛矛醇 |
(-) |
- |
- |
(-) |
- |
|
|
核糖醇 |
(-) |
- |
+ |
- |
- |
|
|
棉子糖 |
+ |
+ |
+ |
v |
+ |
|
|
D-山梨醇 |
+ |
- |
+ |
v |
- |
|
|
α-甲基-D-葡萄糖苷 |
(+) |
+ |
- |
- |
- |
|
|
D-阿拉伯糖 |
(-) |
- |
+ |
- |
+ |
|
|
黃色素 |
- |
+ |
- |
(+) |
- |
|
|
注:+:90%~100%陽性;(+):75%~89%陽性;v:25%~74%陽性;(-):10%~24%陽性;-:0%~9%陽性 |
||||||

圖6 確證生化試驗結果
4.1.9 計算MPN值,根據每一稀釋度檢出的陰溝腸杆菌的結果查MPN表(見表2),計算並報告每100g樣品中的陰溝腸杆菌的最近似值。
4.2陰溝腸杆菌定性檢驗
4.2.1 檢驗樣品中是否有陰溝腸杆菌,檢驗需100g樣品。
4.2.2 取樣前消毒樣品包裝的開啟處和取樣勺,無菌稱取樣品100g至2L的樣品稀釋瓶中,加入900mL預熱到45℃的滅菌蒸餾水,或將樣品直接稱量到裝有9倍預熱到45℃的滅菌蒸餾水的樣品稀釋瓶中,振搖使樣品充分混勻,36℃±1℃培養18h~22h。
4.2.3 移取培養18h~22h的懸液各10mL加入90mL EE肉湯中,36℃±1℃培養18h~22h。
4.2.4 操作同4.1.4~4.1.8。
4.2.5 根據檢驗結果,報告每100 g樣品中是否檢出陰溝腸杆菌。
表2 最可能數(MPN)表(95%置信區間)
使用三管法,接種量分別為10.0g,1.0g和0.1g。
|
陽性管數 |
MPN /100g |
可信限 |
陽性管數 |
MPN /100g |
可信限 |
||||||
|
10 |
1 |
0.1 |
低 |
高 |
10 |
1 |
0.1 |
低 |
高 |
||
|
0 |
0 |
0 |
<3.0 |
- |
9.5 |
2 |
2 |
0 |
21 |
4.5 |
42 |
|
0 |
0 |
1 |
3.0 |
0.15 |
9.6 |
2 |
2 |
1 |
28 |
8.7 |
94 |
|
0 |
1 |
0 |
3.0 |
0.15 |
11 |
2 |
2 |
2 |
35 |
8.7 |
94 |
|
0 |
1 |
1 |
6.1 |
1.2 |
18 |
2 |
3 |
0 |
29 |
8.7 |
94 |
|
0 |
2 |
0 |
6.2 |
1.2 |
18 |
2 |
3 |
1 |
36 |
8.7 |
94 |
|
0 |
3 |
0 |
9.4 |
3.6 |
38 |
3 |
0 |
0 |
23 |
4.6 |
94 |
|
1 |
0 |
0 |
3.6 |
0.17 |
18 |
3 |
0 |
1 |
38 |
8.7 |
110 |
|
1 |
0 |
1 |
7.2 |
1.3 |
18 |
3 |
0 |
2 |
64 |
17 |
180 |
|
1 |
0 |
2 |
11 |
3.6 |
38 |
3 |
1 |
0 |
43 |
9 |
180 |
|
1 |
1 |
0 |
7.4 |
1.3 |
20 |
3 |
1 |
1 |
75 |
17 |
200 |
|
1 |
1 |
1 |
11 |
3.6 |
38 |
3 |
1 |
2 |
120 |
37 |
420 |
|
1 |
2 |
0 |
11 |
3.6 |
42 |
3 |
1 |
3 |
160 |
40 |
420 |
|
1 |
2 |
1 |
15 |
4.5 |
42 |
3 |
2 |
0 |
93 |
18 |
420 |
|
1 |
3 |
0 |
16 |
4.5 |
42 |
3 |
2 |
1 |
150 |
37 |
420 |
|
2 |
0 |
0 |
9.2 |
4.4 |
38 |
3 |
2 |
2 |
210 |
40 |
430 |
|
2 |
0 |
1 |
14 |
3.6 |
42 |
3 |
2 |
3 |
290 |
90 |
1000 |
|
2 |
0 |
2 |
20 |
4.5 |
42 |
3 |
3 |
0 |
240 |
42 |
1000 |
|
2 |
1 |
0 |
15 |
3.7 |
42 |
3 |
3 |
1 |
460 |
90 |
2000 |
|
2 |
1 |
1 |
20 |
4.5 |
42 |
3 |
3 |
2 |
1100 |
180 |
4100 |
|
2 |
1 |
2 |
27 |
8.7 |
91 |
3 |
3 |
3 |
>1100 |
420 |
- |
|
注:如果接種量擴大10倍,分別為100.0 g,10.0 g和1 g時,表中的數字相應縮小10倍。如果接種量縮小10倍,分別為1.0 g,0.1 g和0.01 g時,表中的數字相應擴大10倍,其餘類推。 |
|||||||||||
相關標準:
SN/T 2552.7-2010 乳與乳製品衛生微生物學檢驗方法 第7部分 陰溝腸杆菌檢驗 -標準下載
相關產品:
注:本文屬betway必威西汉姆联生物原創,未經允許不得轉載。
上一篇:檸檬酸杆菌的檢驗方法及結果判斷

