











一、大腸菌群簡介
大腸菌群是革蘭氏陰性、無芽孢、氧化酶陰性的杆狀細菌,為需氧和兼性厭氧,可在有膽鹽(或具有其他抑製生長的表麵活性劑)存在的情況下生長,通常可在36℃士2℃發酵乳糖並產酸和醛。主要由腸杆菌科中四個屬內的一些細菌所組成,即埃希氏菌屬、檸檬酸杆菌屬、克雷伯氏菌屬以及腸杆菌屬。
大腸菌群主要來源於人畜糞便,故以此作為糞便汙染指標來評價食品的衛生質量,推斷食品中有否汙染腸道致病菌的可能。如果大腸菌群存在於食品中,表明未作有效的消毒處理、加工後保存條件不良或消毒後又受到汙染。快速檢驗這些細菌,有助於食品的衛生管理,維護消費者的食用安全。
二、參考標準
《GB8538-2016 飲用天然礦泉水:大腸菌群檢驗》
三、檢驗原理
3.1 多管發酵法
根據大腸菌群細菌具有的生物特性,如革蘭氏陰性無芽孢杆菌,在37℃培養24h能發酵乳糖並產氣的特點,將不同量的水樣接種到含乳糖的培養基中,經培養後根據陽性反應結果可測出原水樣中大腸菌群的最可能數(MPN)。
3.2 濾膜法
采用孔徑為0.45μm水相微孔薄膜,將水中所含的細菌截留在濾膜上,然後將濾膜貼在選擇性鑒別培養基上,經37℃培養24h後,大腸菌群細菌在濾膜上長出具有特征性的菌落,直接計數典型菌落數,計算出每100mL水樣中所含的大腸菌群數。
大腸菌群可產生β-半乳糖苷酶,分解培養基中的酶底物-茜素-β-D-半乳糖苷(以下簡稱Aliz-gal),使茜素遊離並與固體培養基中的鋁、鉀、鐵、銨離子結合形成紫色(或紅色)的鼇合物,使菌落呈現相應的顏色。
四、檢驗方法以及結果分析
4.1 多管發酵法
大腸菌群多管發酵法檢驗程序見圖1。
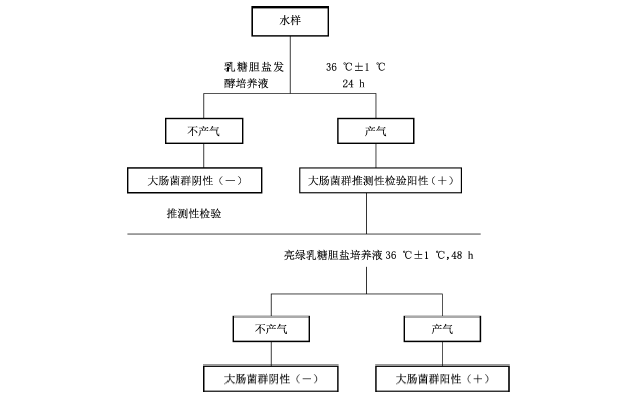
圖1 大腸菌群檢驗程序
4.1.1 礦泉水水源水檢測
4.1.1.1 推測性檢驗
a) 吸取10mL水樣接種到盛有10mL雙料乳糖膽鹽發酵培養液的試管中,共接種5份;
b) 吸取1mL水樣接種到盛有10mL單料乳糖膽鹽發酵培養液的試管中,共接種5份;
c) 吸取1mL水樣接種到9mL滅菌生理鹽水的試管中,混勻,用5mL滅菌吸管吸取5mL稀釋液,分別加到5支盛有10mL單料乳糖膽鹽發酵培養液的試管中,每管1mL(即0.1mL水樣);
d) 輕搖試管,使液體充分混合,置36℃±1℃培養箱內培養25h。觀察每管是否產氣,若有氣體產生該管則為推測性檢驗陽性,如不產氣則為大腸菌群陰性。
質控菌株接種到乳糖膽鹽發酵培養基管中,培養結果如下圖所示:

圖2 標準菌株在乳糖膽鹽發酵培養基中生長情況
4.1.1.2 確證性試驗
a) 自推測性檢驗陽性管中取一接種環培養液,接種到亮綠乳糖膽鹽培養液(BGLB)管中,置36℃±1℃培養箱中培養48h;
b) 觀察BGLB管中的產氣情況,如有氣體產生,就可確定為“大腸菌群陽性”;如無氣體產生則為“大腸菌群陰性”。記下BGLB管裏產氣的陽性試管數,查MPN表可得出水樣中大腸菌群的MPN值。
質控菌株接種到BGLB管中,培養結果如下圖所示:

圖3 大腸菌群在BGLB肉湯中生長情況
4.1.1.3 MPN值的計算
如水樣含菌量少,也可按100mL、10mL、1mL接種,那麽其實際MPN值應為表中的MPN值除以10;反之如含菌量較多,也可接種1mL、0.1mL、0.01mL,其實際MPN值應為表中的MPN值乘以10,餘此類推。
4.1.1.4 列舉說明
假設推測性檢驗15支試管中的陽性管數如下:①在接種量為10mL的管中有5支管陽性;②在接種量為1mL的管中有4支管陽性;③在接種量為0.1mL的管中有2支管陽性;
作為推測性檢驗結果為5-4-2。當把以上陽性管轉種到BGLB管裏,經培養後,作為證實性檢驗所給的結果如為5-3-1,那麽查MPN表,就可知大腸菌群的MPN值為每100mL水樣中110。接種量為100mL、10mL、1mL時,MPN值為11。如接種量為1mL、0.1mL、0.01mL時,MPN值即為1100。
表1 大腸菌群(MPN)檢索表(部分)
(總接種量55.5mL,其中5份10mL水樣、5份1mL水樣、5份0.1mL水樣)

4.1.2 直接飲用的礦泉水的檢測
礦泉水出廠成品水或準備直接飲用的礦泉水,一般不應有汙染,需要經常檢驗,可按下法進行接種。
4.1.2.1 推測性檢驗
a) 用10mL的滅菌吸管向5支盛有10mL雙料乳糖膽鹽發酵培養液的試管中,每管接種10mL水樣。
b) 置36℃±1℃培養箱中培養24h,觀察每支管的產氣情況,如有氣體產生,則認為推測性檢驗陽性。
4.1.2.2 確證性試驗
操作步驟同礦泉水水源水檢驗。
4.1.2.3 MPN值的計算
當經過證實性檢驗後,5管10mL水樣結果中,陽性反應的管數對應的MPN 值及其95%的可信限範圍見表2。
表2 用5管10mL水樣時各種陽性和陰性結果組合的MPN值及其95%的可信限
|
陽性反應管數 |
MPN/100mL |
95%可信限 |
|
|
下限 |
上限 |
||
|
0 |
0 |
0 |
6.0 |
|
1 |
2.2 |
0.1 |
12.6 |
|
2 |
5.1 |
0.5 |
19.2 |
|
3 |
9.2 |
1.6 |
29.4 |
|
4 |
16 |
3.3 |
56.9 |
|
5 |
>16 |
8.0 |
無限 |
4.2 濾膜法
4.2.1 操作步驟
4.2.1.1 用滅菌鑷子夾取滅菌濾膜邊緣部分,將粗糙麵向上,貼放在已滅菌的濾床上,固定好濾器,將100mL水樣(如水樣含菌數較多,可減少過濾水樣量,或將水樣稀釋)注入濾器中,打開濾器閥門,在-5.07×104 Pa(負0.5大氣壓)下抽濾。
4.2.1.2 水樣濾完後,再抽氣約5s,關上濾器閥門,取下濾器,用滅菌鑷子夾取濾膜邊緣部分,移放在品紅亞硫酸鈉培養基上,濾膜截留細菌麵向上,濾膜應與培養基完全貼緊,兩者間不得留有氣泡,然後將平皿倒置,放入36℃±1℃恒溫箱內培養24h±2h。
4.2.1.3 觀察濾膜上麵的菌落特征。大腸菌群典型菌落在遠藤培養基上具有以下特征:
a) 紫紅色,具有金屬光澤的菌落;
b) 深紅色,不帶或略帶金屬光澤的菌落;
c) 淡紅色,中心色較深的菌落;
d) 挑取不少於3個(不足3個則全挑)可疑菌落,進行革蘭氏染色鏡檢觀察。
質控菌株接種到品紅亞硫酸鈉培養基平板上,培養結果如下圖所示:
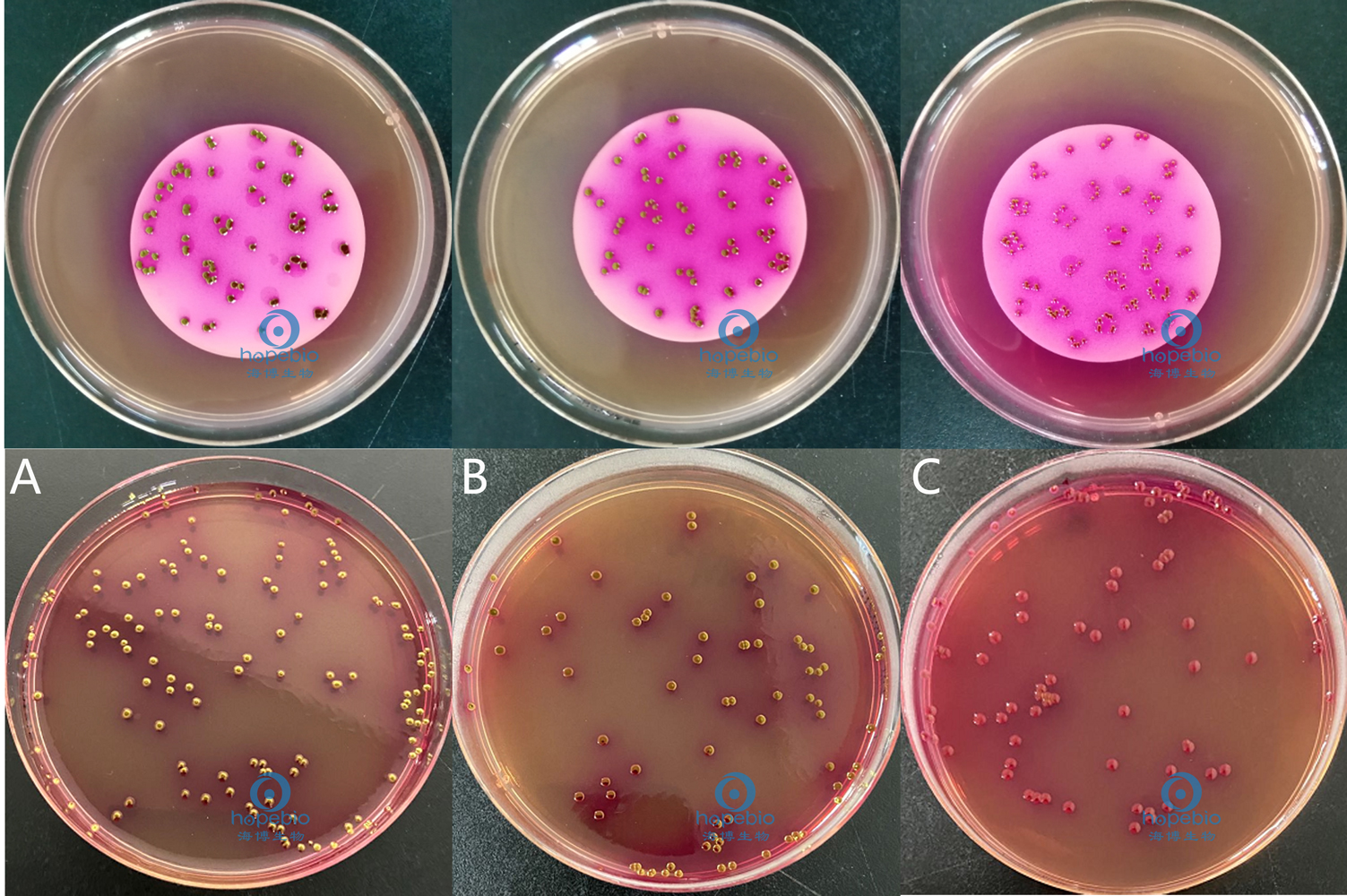
圖4 大腸菌群在品紅亞硫酸鈉培養基平板上生長情況
注:A:大腸埃希氏菌ATCC 25922;B:大腸埃希氏菌ATCC 8739;C:弗氏檸檬酸杆菌ATCC 43864
4.2.1.4 凡係革蘭氏陰性無芽孢杆菌,再接種乳糖蛋白腖培養液,經36℃±1℃培養24h±2h後,如產酸產氣則判定為大腸菌群陽性。

圖5 大腸埃希氏菌ATCC 25922革蘭氏染色鏡檢結果

圖6 質控菌株在乳糖蛋白腖培養液中生長情況
4.2.2 結果與報告
濾膜上的大腸菌群菌落數按下列公式計算,以每100mL水樣中的大腸菌群數報告結果:
每100mL水樣中大腸菌群菌落數(CFU/100mL)=確證為大腸菌群菌落數(CFU)×100/過濾的試樣量(mL)
舉例說明:
濾膜上有100個典型菌落,挑取10個典型菌落(可疑菌落)做革蘭氏染色鏡檢,發現有8個菌落為革蘭氏陰性無芽孢杆菌,這8個菌落接種乳糖蛋白腖培養液,培養後,有6支管產酸產氣,為大腸菌群陽性。
則每100mL水樣中大腸菌群菌落數為:(100×6/10×100)/100=60(CFU/100mL)
相關產品:
注:本文屬betway必威西汉姆联生物原創,未經允許不得轉載。
上一篇:大腸菌群的快速檢測方法及結果判斷

